
Les capteurs magnétiques à base d’électronique de spin à magnétorésistance géante (GMR) présentent l’avantage d’avoir une très grande sensibilité, de l’ordre de 50 à 200 pT/√Hz, d’être peu coûteux et de pouvoir être facilement intégrés. Ils sont notamment à l'origine de l'accroissement spectaculaire de la capacité des disques durs pour le stockage magnétique de l'information.
Il est aussi possible d'intégrer ce type de capteurs performants dans des dispositifs d'analyse sur puce, pour des applications en biologie (lab-on-chip). La détection magnétique d'objets marqués peut être théoriquement réalisée au sein de n’importe quelle matrice complexe et sans étape de lavage des échantillons. Autre avantage, la biopuce magnétique permet l’étude, même en très faible quantité, de cibles biologiques de toutes tailles (cellules, bactéries etc..), alors que des tests de référence de type « bandelettes » peuvent manquer de sensibilité pour détecter cellules et bactéries (du, entre autre, à leur difficulté de migration le long de la bandelette).
Pour détecter des objets biologiques, naturellement non magnétiques, tels que des cellules de myélome murin utilisées comme modèle d’étude, celles-ci sont préalablement marqués au SPI/LERI avec des billes magnétiques fonctionnalisées par des anticorps monoclonaux ayant pour cible l'antigène biologique d’intérêt, exprimé à la surface des cellules. Les objets biologiques ainsi marqués circulent dans un canal microfluidique. Les billes sont alors aimantées avec un aimant permanent et c'est leur champ dipolaire qui est ensuite détecté lors de leur passage au-dessus d'un capteur GMR (figure 1). Un signal est donc obtenu à chaque passage à proximité du capteur GMR d’une cellule magnétiquement marquée.
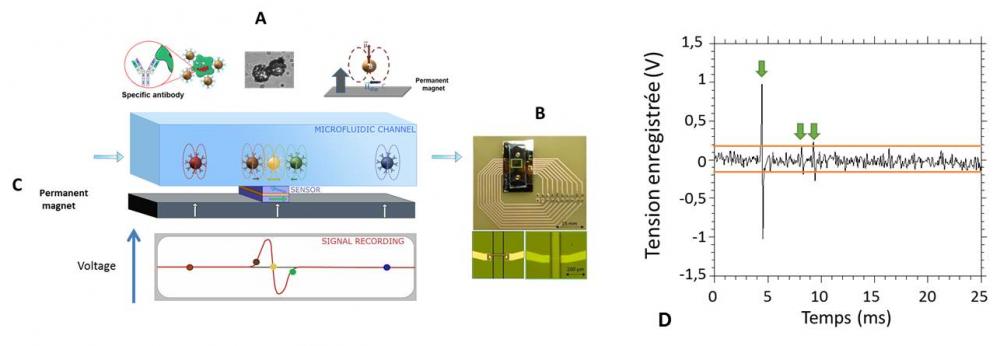
Cette étude, a été réalisée dans le cadre de la thèse de Manon Giraud, avec un premier prototype de laboratoire sur puce, composé d’un canal microfluidique situé au-dessus d’une série de capteurs GMR. Elle a permis d’évaluer pour la première fois les performances du dispositif en termes de sensibilité, spécificité, répétabilité, robustesse, rapidité et facilité d’utilisation.
La sensibilité (ou limite de détection) otenue de 3×104 cellules/mL s'avère légèrement inférieure à celle de tests classiquement effectués en laboratoire au LERI par test ELISA (Enzyme Linked Immunosorbent Assay) ou par cytométrie en flux. Mais le test ainsi réalisé peut encore être optimisé, et, de biens meilleures performances peuvent être attendues, en discriminant mieux les signaux spécifiques des cellules marquées, de ceux issus de billes magnétiques individuelles et libres ou encore d’éventuels agrégats de billes.
Un nouveau prototype de biopuce breveté a alors été conçu et breveté, où 2 séries de capteurs sont placés de part et d’autre du canal microfluidique (figure 2). La corrélation des mesures permet d’obtenir la position, la vitesse et le moment magnétique des objets doublement détectés. Ceci permet de bien mieux distinguer le signal issu des objets biologiques marqués, de celui issu des billes surnuméraires ou des éventuels agrégats.
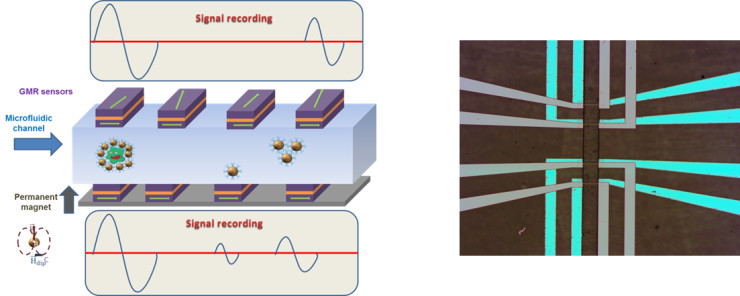
L’utilisation de billes avec une grande stabilité colloïdale, spécialement synthétisées pour ce projet par le laboratoire PHENIX (PHysicochimie des Electrolytes et Nanosystèmes InterfaciauX, UMR 8234 CNRS – Université Sorbonne), devrait permettre d'obtenir une meilleure dispersion des billes, réduisant ainsi considérablement le nombre d’agrégats. Comparé aux tests de référence, une bien meilleure sensibilité dans la détection de cellules individuelles est ainsi attendue.
Contact CEA :
- Guénaëlle Jasmin-Lebras, Laboratoire Nanomagnétisme et Oxydes (SPEC/LNO)
- Stéphanie Simon, Laboratoire d'Études et Recherches en Immunoanalyse (JOLIOT/DMTS/SPI/LERI).
- Cécile Féraudet Tarisse Laboratoire d'Études et Recherches en Immunoanalyse (JOLIOT/DMTS/SPI/LERI).
Référence:
Manon Giraud : « Mise au point d’un laboratoire sur puce pour la détection de cellules eucaryotes par des capteurs à magnétorésistance géante« , thèse de l'Université Paris-Saclay.
Evaluation of in-flow magnetoresistive chip cell-counter as a diagnostic tool
M. Giraud, F.D. Delapierre, A. Wijkhuisen, P. Bonville, M. Thévenin, G. Cannies, M. Plaisance, E. Paul, E. Ezan, S. Simon , C. Fermon , C. Féraudet-Tarisse and G. Jasmin-Lebras, Biosensors 2019, 9(3), 105.
Brevet Français n° 1855217, C. Fermon, M. Giraud, F.D. Delapierre, G. Jasmin.
Voir l'actualité de l'Institut Joliot : « Des capteurs magnétiques pour des biopuces ultra-sensibles« .
Collaboration:
-
Service de Physique de l'État Condensé (SPEC), UMR 3680 CEA – CNRS, Université Paris-Saclay
M. Giraud, F.D. Delapierre, G. Jasmin, G. Cannies, Elodie Paul et C. Fermon -
Service de Pharmacologie et d’Immunoanalyse (SPI), Laboratoire d'Études et Recherches en Immunoanalyse (LERI), CEA, INRA, Université Paris-Saclay
C. Féraudet Tarisse, A. Wijkhuisen, M. Plaisance et S. Simon.



