Au CIMAP, l’exploration des effets biologiques des irradiations à ultra-haut débit de dose éclaire les mécanismes encore débattus de l’effet FLASH, ouvrant de nouvelles perspectives pour améliorer la radiothérapie des cancers.
La radiothérapie dite FLASH, reposant sur des débits de dose ultra-élevés (supérieurs à 50 Gy/s), suscite un intérêt croissant en raison de sa capacité à préserver les tissus sains tout en maintenant l’efficacité antitumorale. Pourtant, les mécanismes à l’origine de cet effet restent mal compris, en particulier aux débits encore plus élevés. Le principal verrou scientifique réside dans le manque de données expérimentales couvrant une large gamme de débits de dose et intégrant plusieurs indicateurs biologiques pertinents.
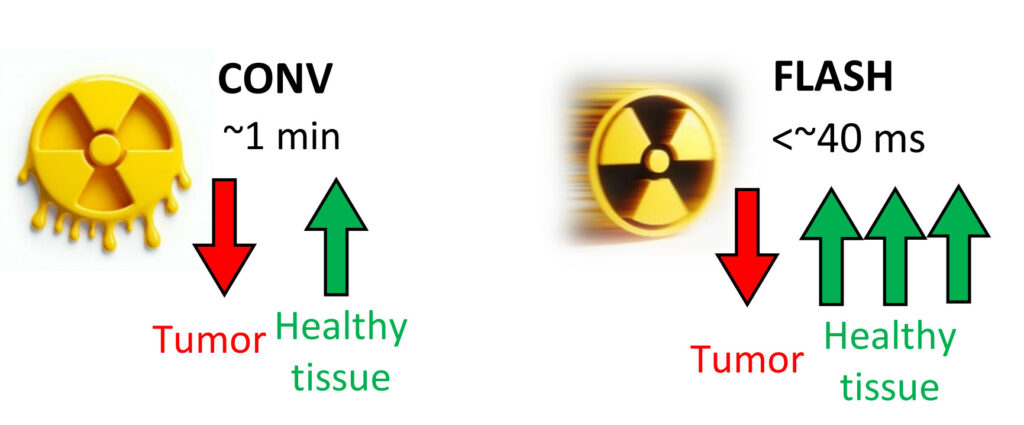
Dans cette étude in vitro, des cellules tumorales du cerveau (glioblastome U251) et du poumon (carcinome A549), ainsi que leurs équivalents sains, ont été irradiées par faisceau de protons sur une large plage de débits, de 4 Gy/min à 1250 Gy/s, pour des doses comprises entre 2 et 10 Gy. Les résultats montrent une diminution de la survie des cellules cancéreuses aux débits les plus élevés, notamment à 1250 Gy/s, suggérant un gain thérapeutique potentiel accru. Parallèlement, l’analyse du cycle cellulaire révèle que les cellules saines présentent davantage un arrêt transitoire du cycle cellulaire (phase G2), un mécanisme souvent associé à la réparation des dommages, indépendamment du débit de dose mais plus marqué lorsque la dose augmente.
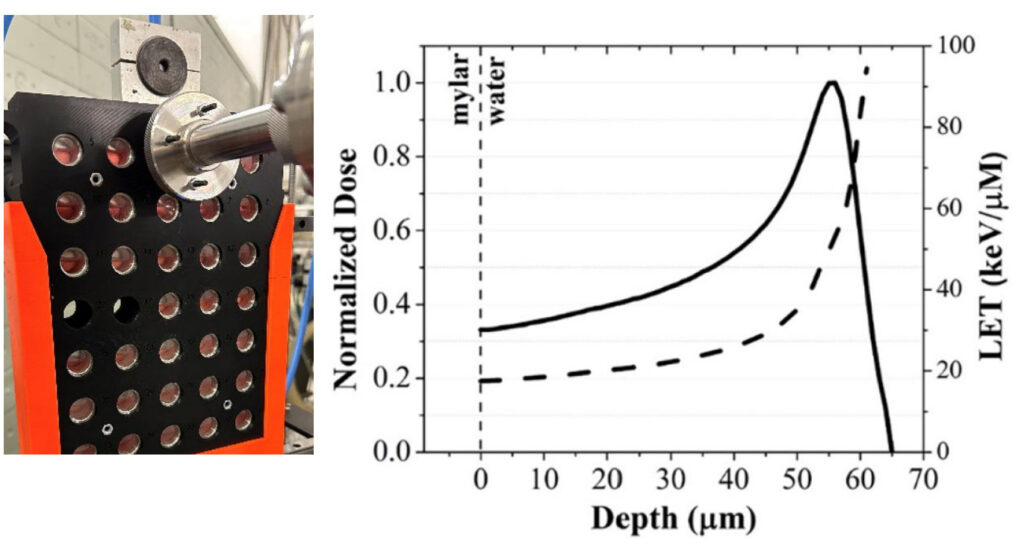
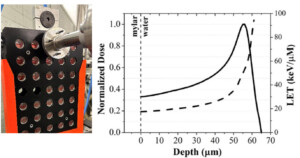
Configuration d’irradiation et courbe profondeur-dose avec LET
Un apport majeur de ces travaux concerne la production d’espèces réactives de l’oxygène (ROS), impliquées dans les dommages cellulaires. Les résultats montrent que leur formation est maximale au débit conventionnel (4 Gy/min) et diminue lorsque le débit augmente. De plus, les cellules saines présentent systématiquement des niveaux de ROS plus élevés que les cellules tumorales. Ces observations suggèrent que la modulation des ROS pourrait contribuer aux mécanismes impliqués dans l’effet FLASH.
Ces résultats apportent un éclairage nouveau sur les mécanismes différenciés entre cellules saines et tumorales sous irradiation à très haut débit. Ils renforcent l’hypothèse d’un bénéfice thérapeutique accru à des débits extrêmes, tout en soulignant la complexité des processus biologiques en jeu. À terme, ces travaux ouvrent la voie à une optimisation fine des paramètres d’irradiation en radiothérapie FLASH, en vue d’optimiser, à plus long terme, les stratégies de radiothérapie FLASH.
Référence
« In vitro flash effect as a function of ultra-high dose rates with proton beam », Mihaela Temelie, Mateusz Sitarz, Mihaela Tudor, Kilian Lecrosnier, Mihai Radu, Diana Savu, François Chevalier, International Journal of Particle Therapy 17 (2025) 101053 – hal-05397419.
Collaboration
Contact CEA
- CIMAP : François Chevalier, Kilian Lecrosnier
- LIDYL : Gérard Baldacchino