L’hydrogène a une densité énergétique massique importante : 120 MJ/kg, soit près de trois fois celle des hydrocarbures. Cette caractéristique fait de l’hydrogène un excellent support de stockage d’énergie, en particulier dans le cadre de la transition énergétique qui s’appuie pour une part sur des énergies renouvelables bas-carbone, mais intermittentes (solaire, éolien) L’hydrogène présente cependant une densité d’énergie volumique faible, et nécessite d’être concentré en volume, en attendant son utilisation. Les méthodes de stockage usuelles sous forme gazeuse (compression) ou liquide (liquéfaction à basse température) aujourd’hui utilisées posent des limites en termes d’efficacité, et exigent certaines précautions de sécurité.
Le stockage chimique, est une autre voie pour stocker l’hydrogène de manière réversible. Dans ce but, les hydrures de bore, présentent une forte densité énergétique et leur stabilité thermique les rendent attrayants pour ces applications de stockage d’énergie, mais leur utilisation en cycle nécessite de savoir les régénérer.
L’équipe du NIMBE/LCMCE propose une nouvelle voie de synthèse applicable à la régénération d’hydrures de bore, par hydrogénolyse de précurseurs chlorés, produits intermédiaires dans le cycle du stockage de l’hydrogène dans des matériaux à base de bore. Cette méthode repose sur des conditions « douces » : 25°C et 10 bar d’hydrogène, comparé aux procédés industriels sur lesquels repose la synthèse des hydrures de bore aujourd’hui.
Le stockage chimique, qui lie l’hydrogène à d’autres molécules, facilite son transport et son utilisation et les hydrures de bore sont une solution innovante pour stocker l’hydrogène de manière réversible. Leur forte densité énergétique et leur stabilité thermique les rendent attrayants pour des applications mobiles et stationnaires, comme les voitures à pile à combustible et les systèmes de stockage d’énergie renouvelable. Bien que la libération de l’hydrogène à partir de ces matériaux soit bien étudiée, aucun procédé n’est encore opérationnel. L’un des verrous technologiques au déploiement de cette technologie, et sur lequel les efforts de recherche se poursuivent, est la régénération des hydrures de bore, générés à partir des sous-produits (oxydes de bore, nitrure de bore BN) issus de la libération de l’hydrogène. Une des étapes nécessaires pour obtenir une utilisation durable et efficace de ces matériaux.
Les hydrures de bore, notamment l’ammonia-borane (NH3-BH3) et les borohydrures (BH4−), en particulier ceux de métaux alcalins (LiBH4, NaBH4) sont des matériaux stables permettant de stocker une quantité importante d’hydrogène en proportion massique (19.5% wtH2 pour NH3.BH3, 19 wtH2% pour LiBH4). Actuellement très utilisés pour leurs propriétés réductrices dans de nombreux procédés industriels ainsi qu’en chimie de synthèse, leur utilisation pour le stockage de l’hydrogène a été envisagée avec le développement des piles à combustibles, mais se heurte au défi que représente leur synthèse : à l’échelle industrielle la préparation des hydrures de bore repose principalement sur des procédés à haute température de type Brown-Schlesinger ou Bayer, qui nécessitent l’utilisation de métaux alcalins (sodium métal) qui pèsent sur le bilan énergétique. La très faible efficacité énergétique de ces procédés empêche d’envisager un stockage réversible de l’hydrogène avec ces composés. Ceci implique également la régénération des sous-produits issus de l’extraction de l’hydrogène comme par exemple des borazines (B3N3H6) ou des oxydes de bore.
Dans le cadre de la thèse de Guilhem Zwart réalisée au Laboratoire de Chimie Moléculaire et de Catalyse pour l’Énergie (NIMBE/LCMCE), l’équipe a travaillé sur une des étapes de cette régénération, avec la réalisation de la première synthèse d’hydrures de bore par hydrogénolyse de précurseurs chlorés dans des conditions douces : 25°C et 10 bar d’hydrogène. Cette méthode s’affranchit de l’utilisation de réducteurs forts et repose sur l’activation de l’hydrogène par le composé de bore avec l’assistance de triéthylamine (Et3N : N(CH2CH3)3 ), une base abondante. Cette méthode a initialement été développée et optimisée sur des substrats dialkylchloroboranes (R2BCl, où R est un alkyl) avant d’être adaptée pour la préparation de composée à plus haute valeur ajoutée tel que le catecholborane (C6H4O2BH) et le pinacolborane ((CH3)4C2O2BH) utilisés en synthèse organique pour la réduction de liaisons C=O. [1]
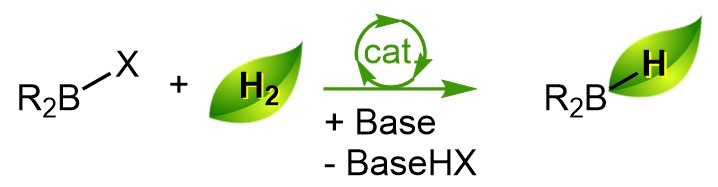
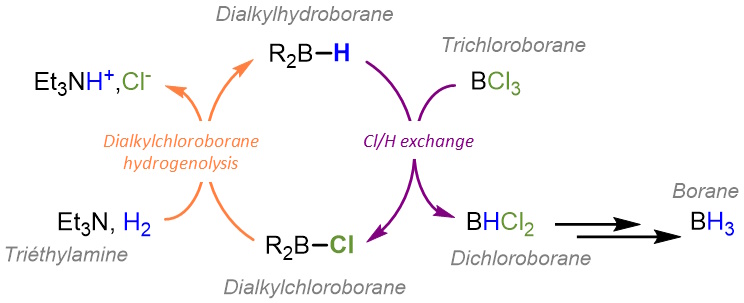
Le trichloroborane (BCl3) en présence de triéthylamine ne permet pas d’activer l’hydrogène dans les conditions initialement décrites, en revanche, des échanges de groupements halogénures/hydrures sur les dérivés du bore sont connus. À partir de ce résultat l’équipe a donc développé un système catalytique à base de dialkylchloroboranes (R2B-Cl). Lors d’une première étape le dialkylchloroborane est converti en dialkylhydroborane (R2B-H) par hydrogénolyse, i.e. par rupture de la liaison B-Cl par action de l’hydrogène, en présence de la triéthylamine. Un échange chlorure/hydrogène entre le BCl3 et le dialkylhydroborane (R2B-H) conduit aux intermédiaires dichloroborane (HBCl2) et chloroborane (H2BCl) ainsi qu’à régénérer le dialkylchloroborane à partir du dialkylhydroborane pour initier un nouveau cycle catalytique. Cette méthode nécessite cependant de travailler dans des conditions de pression et de température plus dures, jusqu’à 140°C et 50 bar d’hydrogène mais conduit à l’obtention sélective du dichloroborane (HBCl2) ou de chloroborane (H2BCl), deux intermédiaires de la synthèse du borane (BH3), ce dernier n’ayant été observé que dans de faibles proportions (5%).
Ces résultats représentent une avancée pour la production d’hydrures de bore, élément pouvant être utilisé pour fixer l’hydrogène de façon aisément réversible. Ils ont fait l’objet d’une demande de brevet, ainsi que d’un article dans la revue Angewandte Chemie. Ils ont également ouvert la voie à de nouveaux projets collaboratifs avec le financement de la thèse de Lilian Hoareau par le PEPR H2 afin de poursuivre ces recherches sur la synthèse de nouveaux hydrures renouvelables pour le stockage de l’hydrogène.
Références :
[1] “Hydrogenolysis of haloboranes: from synthesis of hydroboranes to formal hydroboration reactions”
G. Zwart, A. Mifleur, G. Durin, E. Nicolas, T. Cantat, Angew. Chem. Int. Ed. 2024 e202411468
[2] Thèse de Guilhem Zwart (2024) : « Hydrogénolyse de (pseudo-)haloboranes et de chlorophosphines«
Contact CEA-IRAMIS : Alexis Mifleur, Laboratoire LCMCE du NIMBE (UMR CEA-CNRS), Université Paris-Saclay.
Nomenclature des produits chimiques rencontrés dans la synthèse :
- Groupe éthyle : –CH2CH3
- Triéthylamine (NEt3 : N(CH2CH3)3 ),
- Dialkylchloroboranes (R2BCl)
- Chloroborane (H2BCl)
- Trichloroborane (BCl3)
- Dichloroborane (HBCl2)
- Borane (BH3)
- Ammonia-borane (NH3.BH3)
- Borohydrure (BH4−)
- Borazines (B₃N₃H₆)
- Catecholborane (C6H4O2BH)
- Pinacolborane ((CH3)4C2O2BH)

