Les batteries à flux redox (RFB) présentent le grand avantage de dissocier la quantité d'énergie stockée et la puissance délivrée. Elles sont donc spécifiquement adaptées au stockage des énergies intermittentes (solaire, éolienne). Dans cette technologie, chaque électrolyte est pompé du réservoir où il est stocké jusqu'à une cellule de conversion où se déroule le processus électrochimique.
Pour optimiser les performances des batteries utilisant des électrolytes organiques, il est important de suivre les processus moléculaires se produisant lors des cycles de charge et décharge, et la résonance magnétique nucléaire (RMN) est un outil de choix pour cela. Idéalement il faudrait que les analyses puissent être réalisées pendant le fonctionnement de la batterie, et au plus proche des électrodes et zones d’échange. C'est ce qui a été réalisé sur un spectromètre du NIMBE/LSDRM, où des techniques de fabrique additive ont permis de réaliser une mini-batterie adaptée à une étude « operando ».

Les batteries à flux redox (RFB) sont aujourd'hui principalement basés sur une technologie utilisant les différents degrés d'oxydation du vanadium, dissous dans une solution d'acide sulfurique. La rareté de l'élément V et l'acidité de l'électrolyte impose la recherche d'autres types de composants actifs d'électrolytes, notamment organiques, tel ceux présentant des groupements électrochimiquement actifs de type quinone, nitroxyle ou viologène…, pour lesquels on souhaite mieux comprendre leur comportement en batterie. La RMN est une des techniques d'analyse pouvant apporter des données très utiles dans ce sens.
En utilisant la fabrication additive, et en capitalisant sur leurs précédentes avancées dans la réalisation de dispositifs alliant micro-détection et fluidique, les chercheurs de l’IRAMIS et de l’IRIG sont parvenus à construire une mini-batterie à flux redox à électrolytes organiques s’insérant dans la cavité d’un aimant de spectromètre RMN haute résolution (diamètre maximal utile : 18 mm).
Ce dispositif s’installe sur une base de sonde de micro-imagerie IRM, ce qui permet des expériences de vélocimétrie pour caractériser le flux des solutions électrolytiques durant le fonctionnement de la batterie. Autre avantage : la possibilité ouverte par ce dispositif original de réaliser des analyses localisées par spectroscopie RMN multiéléments (1H et 13C). Ce dernier point est important pour éviter les régions fortement perturbées magnétiquement (au niveau de l’électrode par exemple) et préserver une bonne résolution spectrale. Grâce à ces avancées, il a été possible de répéter des cycles de réduction et d’oxydation d’un électrolyte modèle, la 2,7-anthraquinone disulfonate (AQDS), ce qui a permis de mettre en évidence la dimérisation en milieu acide des espèces oxydée et réduite, ainsi que la formation de l'hétéro-dimère entre les deux espèces.
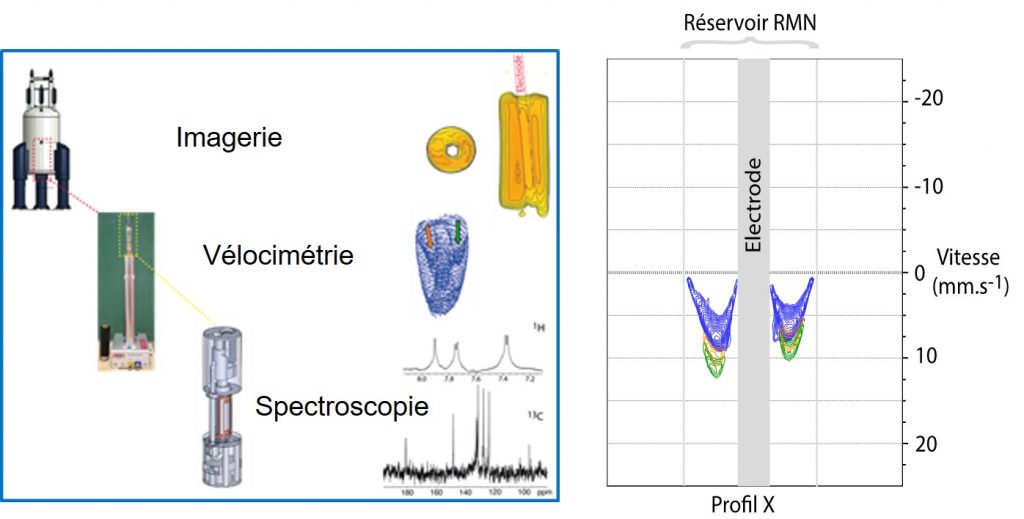
Fig. 1 : À gauche : Véritable « couteau suisse » d’analyse électrochimique, le dispositif principalement imprimé en 3D (diamètre 18 mm) se connecte sur une sonde de micro-imagerie, l'ensemble pouvant être installée au cœur d'un aimant de spectromètre RMN. Il permet à la fois des expériences de spectroscopie multi-noyaux (1H, 13C) à une ou plusieurs dimensions, des expériences d’imagerie et des expériences de diffusion et vélocimétrie.
À droite : expérience de vélocimétrie RMN montrant le profil de vitesse de la solution au sein de la cuve RMN, en fonction du débit de gaz porteur inerte (azote) qui assure l’écoulement du fluide électrolytique en boucle fermée : 1 mL/min (bleu), 2 mL/min (orange), 3 mL/min (vert).
Pour un bon suivi par RMN du fonctionnement de la batterie à flux redox organique, il importe tout d’abord de s’assurer que la circulation de la solution sous l'effet d'une pompe à bulle à gaz inerte, s’effectue correctement. Pour cela, une expérience de vélocimétrie par RMN est réalisée (Voir figure), avant l’enregistrement de chaque spectre RMN.
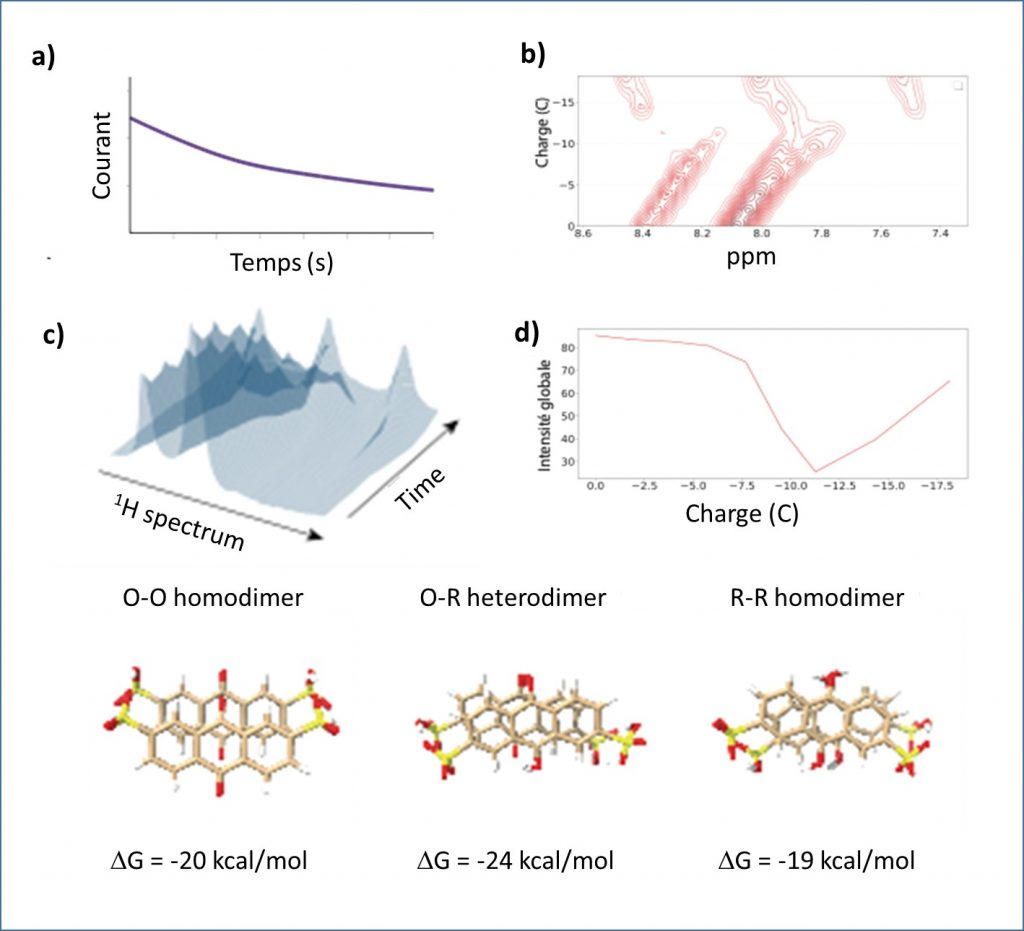
(b) Evolution des spectres RMN 1H au cours de la charge
(c) Représentation 3D de l'évolution des spectres RMN 1H au cours de la charge
d) signal RMN 1H au cours de la charge.
L'évolution des spectres RMN 1H révèle séquentiellement :
- la dimérisation des espèces oxydées (C= O),
- puis le passage par un état paramagnétique (associé à la perte d’intensité en Fig. 3d)
- un spectre intermédiaire composé de 6 signaux 1H pouvant être associés à des composés aromatiques, et attribuée à la formation de l'hétérodimère entre espèces oxydée et réduite.
Enfin, la forme réduite apparaît, caractérisée par 3 signaux 1H bien distincts. De la même façon que la dimérisation entre espèces oxydées O-O est observée, l’homodimère R-R apparaît quand la concentration en espèce réduite augmente. Des calculs basés sur la théorie fonctionnelle de la densité (DFT) confirment également que l’hétérodimère O-R est plus stable que les homodimères (Fig. 3e).
La dimérisation de la molécule active observée au sein de l'électrolyte, première étape d'une éventuelle multimérisation, ne peut qu'entrainer une réduction de la mobilité des molécules actives, une augmentation de la viscosité de l'électrolyte, facteur pouvant limiter les performances de la batterie.
L'ensemble de l'étude montre que grâce au dispositif réalisé il est possible d'obtenir des informations fines en temps réel sur le fonctionnement de la batterie par RMN. Ceci permet des observations très pertinentes pour guider les expériences visant à l'amélioration des performances de ce type d'accumulateurs à flux Redox de forte capacité, indispensables au large développement des sources énergies renouvelables intermittentes (éolien et solaire). Les voies pour éviter la dimérisation observée seront en particulier recherchées.
Le dispositif pouvant être utilisé pour l'analyse in situ d'autres processus électrochimiques par RMN à l'état liquide, plusieurs pistes d'améliorations technologiques de la cellule RMN seront également développées :
- remplacer les inserts en polymère par des inserts en céramique ou en verre imprimés en 3D, chimiquement inertes et plus résistants,
- il est également proposé d'incorporer des microcapteurs de température nécessaires pour optimiser les performances électrochimiques.
Référence :
“Three-dimensional-printed device for in situ monitoring of an organic redox-flow battery via NMR/MRI”
B. Caja-Munoz, K. Chighine, J.-P. Dognon, L. Dubois and P. Berthault, Analytical Chemistry, 95(14) (2023) 6020–6028.
Thèse de Borja Caja-Munoz, « Analyse in situ d’une batterie à flux redox organique par résonance magnétique et fabrication additive« , soutenue le 14/04/2023.
Contacts :
- CEA-IRAMIS : Patrick Berthault (NIMBE/LSDRM)
- CEA-IRIG : Lionel Dubois (IRIG/DIESE/SYMMES/), Grenoble
Collaboration :
- B. Caja-Munoz, K. Chighine, J.-P. Dognon, L. Dubois and P. Berthault, Univ. Paris-Saclay, UMR NIMBE CEA-CNRS, CEA Saclay.
- Lionel Dubois, Univ. Grenoble Alpes, CEA, CNRS, IRIG/SyMMES, UMR 5819, 38000 Grenoble.