|
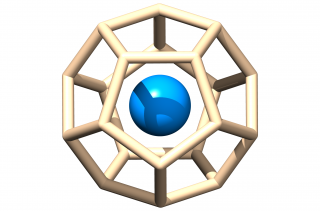
En chimie, les "règles" du doublet, de l'octet et des 18 électrons permettent de concevoir des composés de grande stabilité chimique. Ces règles correspondent au principe de l'occupation complète des orbitales externes de chacun des atomes d'une molécule, soit respectivement s2, (s2, p6) et (s2, p6, d10). Chaque atome dispose ainsi, en partage avec ses voisins, d'une structure électronique externe en couches complètes, de type gaz rare : He, Ar, Ne, Xe et Kr. De la même façon, nous avons montré que des composés avec des liaisons impliquant 32 électrons, avec l'apport des quatorze électrons supplémentaires apportés par des orbitales 5f complètes, pouvaient être très stables. En montrant par des calculs de chimie quantique, la très grande stabilité d'une nouvelle famille de composés impliquant des liaisons à 32 e- entre un atome métallique central (actinide) et une cage ligand (Si20), la simple règle initiale tend à devenir un nouveau principe. Ce travail de recherche fondamentale est mené au Laboratoire de Chimie de Coordination des Éléments f à Saclay (IRAMIS/SIS2M/LCCEf) en collaboration avec le Prof. Pekka Pyykkö (Université d’Helsinki, Finlande) et le Dr. Carine Clavaguéra (CNRS, Ecole Polytechnique, Palaiseau). |