
La modélisation moléculaire est aujourd’hui un des outils principaux de recherche de nouveaux médicaments. En effet, l’étude biologique d’une maladie permet d’identifier les protéines du pathogène ou du corps humain impliquées dans la maladie. On modélise la structure de ces protéines numériquement et on peut ainsi rechercher les meilleures structures chimiques capables de s’y associer et de modifier leur comportement, avant de les synthétiser et de les tester. Les outils de modélisation, soit par les méthodes de chimie quantique soit par des calculs plus empiriques ajustés sur des grandeurs expérimentales (méthodes dites de "champ de force" basées sur potentiels interatomiques paramétrés), doivent donc être très fiables. Il est cependant difficile de les tester pour les améliorer car on manque de données de base, directement comparables avec les prédictions des modèles.
Les chercheurs de l’IRAMIS ont mis au point une technique expérimentale de caractérisation par laser de petites molécules isolées en phase gazeuse, et l’ont appliquée aux peptides, c'est-à-dire de courts segments de protéine de quelques acides aminés. Cette méthode de préparation originale en absence de solvant facilite la comparaison avec les approches théoriques. On peut ainsi observer expérimentalement les formes prévues par les calculs théoriques, ce qui constitue un test sévère pour les algorithmes.
Une modélisation plus fiable des peptides et des protéines devient ainsi possible, ce qui doit permettre à terme d’améliorer les performances des outils de simulation des protéines, tant pour leur structure que pour leur comportement dynamique.
Références :
- Fait marquant IRAMIS oct. 2010 : Synergie expérience-théorie pour la simulation du repliement des protéines
- Gas-Phase Folding of a Two-Residue Model Peptide Chain: On the Importance of an Interplay between Experiment and Theory,
E. Gloaguen, B. de Courcy, J.-P. Piquemal, J. Pilm, O. Parisel, R. Pollet, H. S. Biswal, F. Piuzzi, B. Tardivel, M. Broquier and M. Mons, J. Am. Chem. Soc. 13 (2010) 11860.
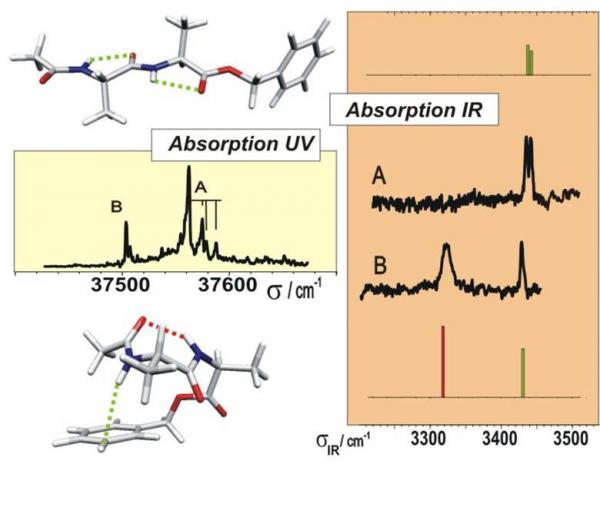
Illustration de la compétition entre formes étendue (en haut) et repliée (en bas) d’un petit peptide, identifiées par leur spectre infrarouge par comparaison avec leur spectre simulé (bâtons). La prédominance des formes étendues (A) par rapport aux formes repliées (B), ainsi mise en évidence, n’est convenablement décrite que par les modèles les plus récents.
•  Physique et chimie pour le vivant et l’environnement › Physique et vivant / Physics and life
Physique et chimie pour le vivant et l’environnement › Physique et vivant / Physics and life
•  Institut Rayonnement Matière de Saclay • Service des Photons Atomes et Molécules
Institut Rayonnement Matière de Saclay • Service des Photons Atomes et Molécules



