Le stress oxydant subi par les divers éléments des cellules biologiques est un facteur important de leur vieillissement. Au-delà du métabolisme naturel, certains stress externes, tels que l'exposition aux UV, aux rayonnements ionisants, aux métaux lourds ou aux nanoparticules, conduisent à la formation d'espèces radicalaires qui sont l’élément déclencheur d'oxydation des composants cellulaires, en particulier les protéines.
Des chercheurs de la DSM (IRAMIS/SIS2M) et de la DSV (IBITECS) apportent un éclairage nouveau sur ces processus d’oxydation impliqués dans le stress oxydant et le vieillissement. Dans un article paru dans Angewandte Chemie [1], ils rapportent l'observation que les radicaux formés lors de l’oxydation des protéines n’étaient pas figés, mais pouvaient migrer entre acide aminés sur des distances nanométriques. Ils montrent ainsi le caractère non local des effets de la formation des espèces radicalaires, et plus particulièrement des conséquences des expositions aux radiations ionisantes.
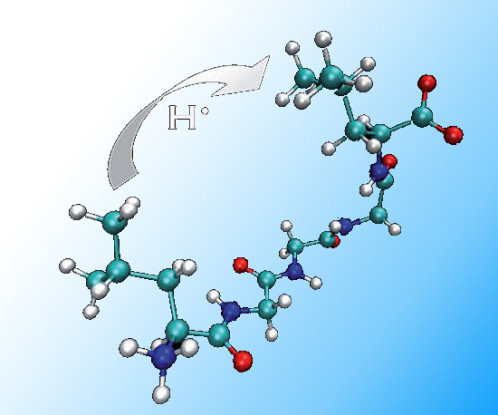
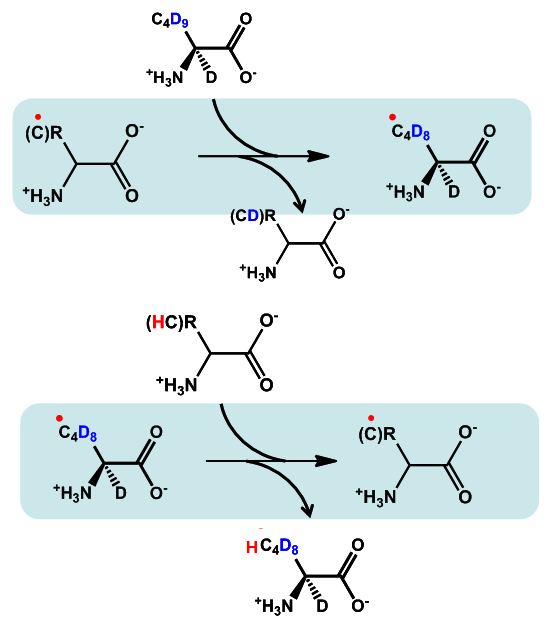
Le processus observé implique des transferts d’atomes H entre radicaux C°, tels que ceux formés lors de l'oxydation initiale. Les réactions présentées sur la figure 1, montrent ce transfert d’hydrogène ou de son isotope, le deutérium, lors de la rencontre de deux acides aminés marqués et non marqués au deutérium (R=C4H10). Ces transferts ont pu être identifiés en couplant radiolyse, marquage isotopique et analyses par spectrométrie de masse. Les observations similaires (figure 2) sur plus de dix acides aminés naturels et sur des peptides modèles montrent toute la généralité du phénomène mis en évidence. Celui-ci pourrait en particulier expliquer la sensibilité particulière de certains sites protéiques à l’oxydation.
Au-delà des premières conclusions de cette étude, nos résultats montrent que la réactivité radicalaire des acides aminés reste encore largement à déchiffrer. Ces recherches doivent aussi pouvoir répondre à des questions plus fondamentales associées à la recherche des origines du vivant, en astrochimie (comment les acides aminés évoluent-ils lorsqu’ils sont exposés au rayonnement présent dans l’espace) ou dans les études de chimie prébiotique (pourquoi et comment les acides aminés utilisés dans les protéines se sont-ils formés).
 |
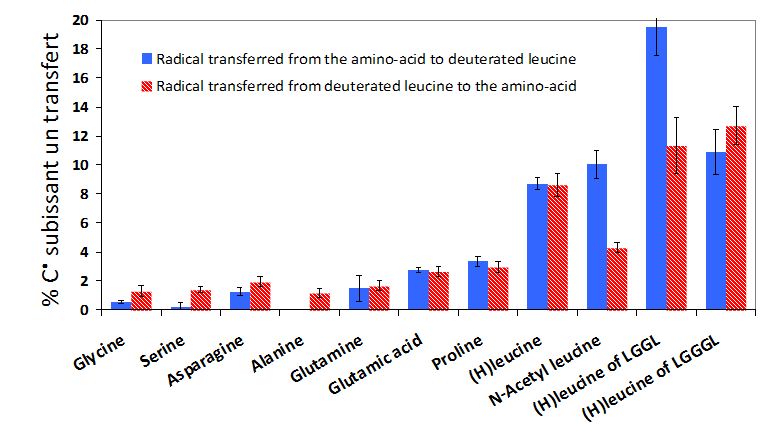 |
| Figure 1 : Transfert possible d’hydrogène et de deutérium entre des acides animés marqués et non marqués au deutérium (R=C4H10). | Figure 2 : Proportion de radical C• formé lors des attaques radicalaires de HO• subissant un transfert de et vers la leucine, en fonction de la nature des partenaires du transfert. |
Références
[1] “Carbon-Centered Radicals can Transfer Hydrogen Atoms between Amino Acid Side Chains”,
Q. Raffy, D.-A. Buisson, J.-C. Cintrat, B. Rousseau, S. Pin, J.P. Renault,
Angew. Chem. Int. Ed. 51(12) (2012) 2960.
Cette action a été soutenue par le réseau CEA de Radiolyse.
Contact : Jean-Philippe Renault (SIS2M/Laboratoire de radiolyse)


