|
L'irradiation des molécules biologiques peut conduire à leur fragmentation et à l'ionisation des fragments. Dans une expérience portant sur l'irradiation par des ions lourds de molécules biologiques (acides aminés : glycine et valine) l'équipe du CIMAP montre l'importance de l'environnement des molécules dans ce processus. Il est observé qu'emprisonnées dans un agrégat permettant une redistribution rapide de l’excès d’énergie, ces molécules peuvent être simplement ionisées, sans fragmentation. |
Les ions multichargés constituent un outil et une sonde pour étudier la physico-chimie des systèmes complexes. Des transferts de charge et d’énergie ont lieu au sein des molécules soumises à un rayonnement ionisant, pouvant induire la rupture de certaines liaisons. L’équipe AMA (Atomes, Molécules, Agrégats) de l’IRAMIS/CIMAP (Centre de Recherche sur les Ions, les Matériaux et la Photonique) à Caen, en collaboration avec l’équipe de physique atomique et moléculaire du KVI à Groningen aux Pays-Bas et le Laboratoire de Physique des Lasers (LPL, Université Paris 13) s’est plus particulièrement intéressée à l’irradiation de biomolécules et à l’effet de l’environnement sur leur fragmentation. Dans ce travail, l’intérêt a été plus spécifiquement porté sur l’irradiation d’acides aminés.
Les études portant sur l’interaction des rayonnements ionisants avec les systèmes d’origine biologique, sont justifiées par l’utilisation, de plus en plus fréquente, en médecine ou dans l’industrie, de faisceaux d’ions ou d’électrons, dans des buts thérapeutiques ou diagnostiques. La compréhension fine des processus induits nécessite alors une analyse poussée des interactions à l’échelle moléculaire [1], rendue difficile par la présence du milieu cellulaire et la complexité des molécules mises en jeu. Dans ce contexte, les recherches effectuées en phase gazeuse permettent de séparer de façon univoque les propriétés intrinsèques des systèmes biomoléculaires, de celles induites par la présence d’un environnement. Depuis peu, il est possible de rendre compte précisément des effets provoqués par les toutes premières couches d’un environnement élémentaire, constitué d’autres molécules biologiques sous forme d’agrégats.
Ce travail s’est porté sur les acides aminés qui sont les unités structurales de base des protéines. Deux d’entre eux font l’objet de cette étude : la glycine (NH2CH2COOH) et la valine ((NH2) (CH)2 (CH3)2COOH), en tant que molécules isolées et de molécules au sein d’un agrégat. A la suite de l'interaction avec des ions multichargés (Xe20+ à 300 keV) les écarts entre les différentes voies de fragmentation sont comparés afin de comprendre l’influence de l’environnement sur le comportement des molécules sous irradiation.
Ces expériences ont été réalisées sur la ligne d’ions de basse énergie ARIBE (Accélérateurs pour les Recherches avec les Ions de Basses Energies) du GANIL à Caen. Expérimentalement, la mise en phase gazeuse des biomolécules est réalisée par chauffage d’une poudre dans un four. La formation d’agrégats est obtenue par la condensation de la vapeur de biomolécules dans une atmosphère d’hélium gazeux refroidie à la température de l’azote liquide. Les ions multichargés sont générés par une source ECR. Les produits de l’interaction entre les ions et les biomolécules sont analysés en coïncidence par un spectromètre de masse à temps de vol.
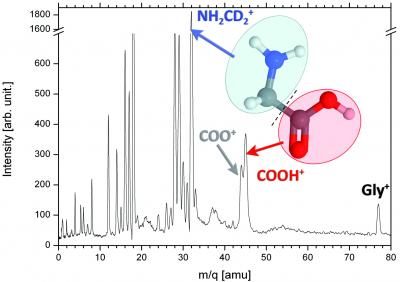
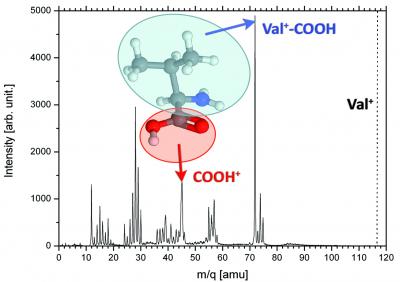
Les ions fortement chargés, ici le Xe20+, fournissent une sonde ultra-brève (femtoseconde) susceptible d’ioniser les molécules à large distance, sans transfert d’énergie. La fragmentation des petits acides aminés est alors gouvernée par la rupture de la liaison C-Cα [2], la colonne vertébrale de la molécule (Figures 1 et 2, fragments [M-COOH]+ et [COOH]+).
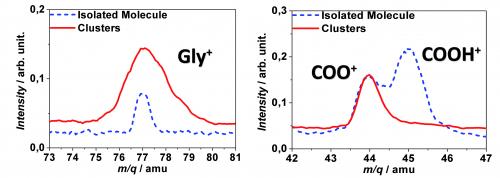
Si l’on considère maintenant les agrégats d’acides aminés, on remarque un élargissement de certains pics tels que celui du cation de glycine (Figure 3 gauche) qui indique un accroissement de d’énergie cinétique. Ceci peut être interprété par la fragmentation des agrégats et donc l'émission de cations de glycine. De manière encore plus nette, on observe un comportement similaire dans le cas de la valine. Alors que la molécule intacte n’est pas détectée dans le cas de la molécule-cible isolée, une proportion importante de cations de valine est mesurée dans le cas des agrégats.
Un autre résultat marquant est la forte diminution, voire la fermeture, des voies de fragmentation correspondant à la rupture de la liaison C-Cα dans le cas des agrégats (par exemple le fragment [COOH]+, figure 3 droite).
On observe donc un effet de l’environnement protecteur de la liaison C-Cα. Cet effet s’explique par la structure de l’agrégat, formé d'un réseau de monomères assemblés par des liaisons hydrogènes. L’excès d’énergie est redistribué sur l’ensemble de l’agrégat menant à la rupture préférentielle des liaisons hydrogène. La fragmentation intermoléculaire permet de dissiper l’énergie évitant ainsi la fragmentation intramoléculaire.
L’agrégat moléculaire agit donc comme un tampon permettant une redistribution rapide de l’excès d’énergie. L’environnement influe donc sur le processus de fragmentation de la molécule [3]. Dans la suite, il est prévu de complexifier davantage l’environnement en formant systèmes nano-hydratés où la molécule d’intérêt est entourée par des molécules d’eau. L’étude de la fragmentation induite par des ions lents est rendu possible par le développement du dispositif PIBALE (Plateforme d’Irradiation de Biomolécules et d’Agrégats Libres et Environnés) financé par le programme Blanc de l’ANR et le Conseil Régional de Basse-Normandie.
Références:
[1] Fundamental processes in radiation damage of DNA
P. Swiderek, Angew. Chem. Int. Ed. 45(25), 4056 (2006).
[2] The mass spectra of the α-amino acids
G. Junk, H. Svec,J. Am. Chem. Soc. 85(7), 839 (1963).
|
[3] Ion-induced fragmentation of amino acids: effect of the environment Contact : Patrick Rousseau (IRAMIS-CIMAP) |
 |