• UMR 3299 - Service Interdisciplinaire sur les Systèmes Moléculaires et les Matériaux
• pas de titre • Laboratoire de Chimie Moléculaire et Catalyse pour l'Energie (LCMCE)


Les contre-ions semblent jouer un rôle important dans la discrimination des ions trivalents des actinides mineurs et des lanthanides au cours des procédés de retraitement des déchets nucléaires. Par exemple, dans la séparation des ions Am(III) et Eu(III) par des oxydes de phosphine, la sélectivité en faveur des ions Am(III) est meilleure en milieu thiocyanate qu'en milieu nitrate. Cette différence a été attribuée au caractère plus mou de l'anion SCN- et à la nature plus covalente de la liaison Am-N (Suresh et al, 2003). La comparaison des structures cristallines de complexes analogues de l'uranium et des lanthanides a permis d'étayer cette hypothèse.
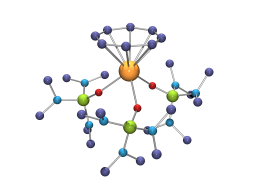
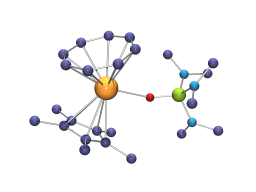
Les structures de [U(η-C8H8)(hmpa)3][BPh4], premier complexe monocyclooctatétraénylique cationique de l'uranium(III), et de ses homologues du samarium et du néodyme montrent que les variations des distances M-C et M-O reflètent simplement celles des rayons ioniques des métaux. Cependant, dans les composés [M(η-C8H8)(η-C5Me5)(hmpa)] (M = Nd, U), les longueurs moyennes des liaison M-C(η-C5Me5) sont identiques, alors que la différence entre les rayons ioniques de U(III) et Nd(III) est égale à 0.04 Å.
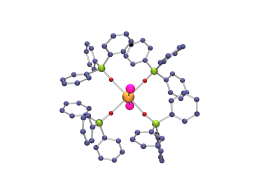
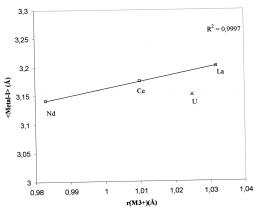
L'étude cristallographique de la série des composés [MX2(OPPh3)4][X] (X = OSO2CF3 et M = Ce, U; X = I et M = Nd, Ce, La, U) montre que la variation des longueurs des liaisons M-O suit celle des rayons ioniques des métaux. En revanche, les distances U-I sont plus courtes que celles prédites par un modèle de liaison purement ionique.
S. M. Cendrowski-Guillaume et al, Eur. J. Inorg. Chem., 2001, 1495-1498.
S. M. Cendrowski-Guillaume et al, Eur. J. Inorg. Chem., 2003, 1388-1393.
J. C. Berthet et al, Polyhedron, 2003, 22, 3475-3482.