Du fait de leur taille, les nanoparticules peuvent interagir avec les éléments du vivant, de la cellule à la molécule biologique. Ceci peut être mis à profit en médecine pour cibler des traitements, mais peut aussi présenter des effets indésirables, lors d'une forte exposition.
Les équipes de l'IRAMIS travaillent selon ces deux voies d'importance sociétale majeure, et plus particulièrement sur :
- Ecotoxicité et nanoparticules (équipes NIMBE/LIONS et /LEDNA)
- Matériaux bio-inspirés
- Nano-médicament
Nanostructures and biomolecules: biomedicine and nanotoxicity
Due to their size, nanoparticles interact with the elementary objects of the living, from cells to biological molecules. This can be used in medicine to target treatments, but can also have undesirable effects at high exposure levels.
IRAMIS teams are working along both of these pathways of major societal importance, mainly on :
- Ecotoxicity and nanoparticles (NIMBE/LIONS and /LEDNA teams)
- Bio-inspired materials
- Nano-medicine
|
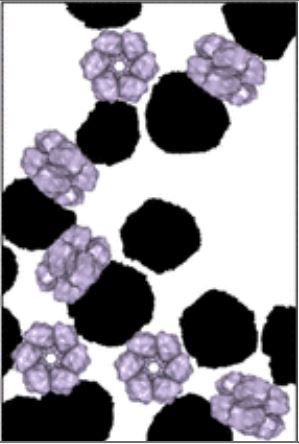
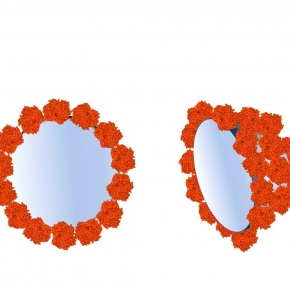
La "corona" désigne l'enveloppe de protéines qui entoure spontanément toute nanoparticule plongée dans un milieu biologique. Elle joue un rôle important dans les mécanismes couramment en jeu en nanomédecine et nanotoxicologie. En étudiant un système modèle de nanoparticules de silice plongées dans une solution d'hémopotéines, il vient d'être montré que les mécanismes d'assemblage de cette corona est fonction de la taille des protéines, ce qui montre la nécessité d'intégrer ce facteur dans les études protéomiques et toxicologiques. |
|
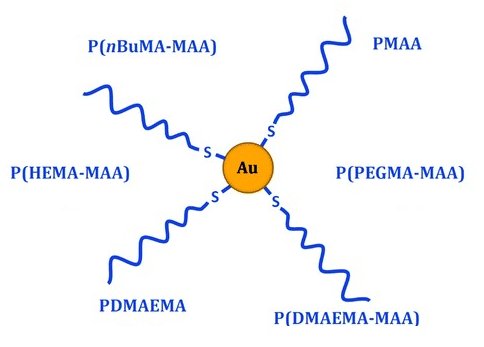
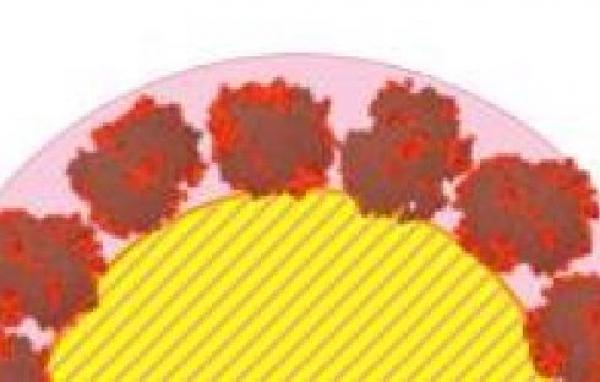
Les nanomédicaments sont considérés comme des thérapies prometteuses pour le traitement du cancer. Cependant, leur utilisation clinique reste encore limitée, dû en partie au fait que leur comportement biologique n'est pas encore vraiment élucidé. Extraire des théories générales à partir de la grande variété de nanoparticules et des conditions de leur utilisation reste en effet difficile, et les techniques pertinentes font défaut pour obtenir des informations in situ. Dans ce travail, ces deux aspects du problème sont abordés en combinant des nanoparticules modèles de nature variable avec des outils in situ basés sur des techniques de diffusion de aux petits angles (SAS, rayons X ou neutrons). La stratégie repose sur le développement d’une bibliothèque de nanoparticules greffées de polymères avec des cœurs d’or identiques, afin de réaliser une étude systématique de leurs interactions avec les systèmes biologiques. Il est ainsi montré qu'une modulation de la chimie des polymères modifie les propriétés de surface, tout en conservant la même structure des nanoparticules, ce qui permet une comparaison fiable entre les objets. Quatre aspects spécifiques ont été plus particulièrement examinés: la stabilité colloïdale, la captation cellulaire, la toxicité et la diffusion dans la matrice extracellulaire. De manière intéressante, il a été montré que la copolymérisation entre les monomères hydrophobes et chargés positivement contribue à réduire significativement la toxicité des nano-objets tout en conservant une bonne internalisation cellulaire. Les techniques SAS ont ainsi fourni des informations précieuses in situ sur l'évolution et la migration des nanoparticules dans des environnements biologiquement pertinents (milieux de culture cellulaire et matrice extracellulaire). [1, 2, 3] 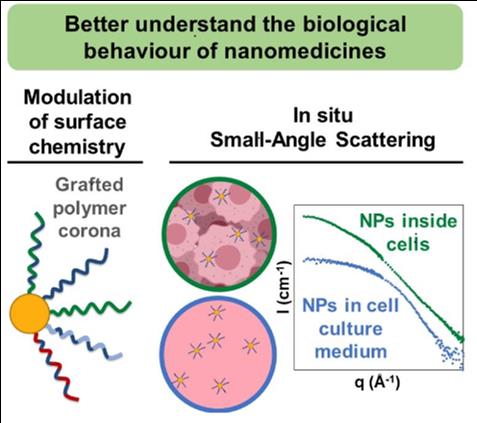 |
|
Formuler un substitut sanguin capable de transporter efficacement l’oxygène, sans toxicité biologique ou chimique, et dont la préparation serait peu coûteuse pour de très grandes quantités, est un graal qui remonte au XVIIème siècle [1]. De nombreuses solutions ont été avancées, notamment à base d’hémoglobines, protéines d’origine humaine, animale ou bactérienne qui transportent l’oxygène dans le sang. Aucune piste n’a permis jusqu’à présent de proposer un produit acceptable par les autorités de santé. Une équipe d'IRAMIS, en collaboration avec deux équipes de l'institut Frédéric Joliot, et avec une jeune start-up : LBP propose une nouvelle voie : Il est montré que la molécule CB5(OH)10 est capable de complexer efficacement dans sa cavité le dioxygène d'une solution physiologique [2]. CB5(OH)10 appartient à la famille des cucurbiturils, en référence à leur forme qui ressemble à celle d'une citrouille. La propriété d'encapsulation du dioxygène par CB5(OH)10 est comparable, en son principe, à celle de l'hémoglobine, principal vecteur de transport du dioxygène dans le sang. La start-up ambitionne de proposer un substitut sanguin entièrement thermostable et synthétique, donc sans aucun risque infectieux. |
| Des chercheurs de l’I2BC@Saclay et de l’UMR NIMBE, en collaboration avec le Laboratoire Léon Brillouin (LLB), ont analysé la structure de la couronne composée de deux protéines modèles adsorbées sur des nanoparticules de silice, en utilisant la technique de diffusion des neutrons aux petits angles. Ils montrent que les structures formées sont de véritables nanoassemblages contrôlés, dans lesquels les protéines conservent leur forme. |
| Une collaboration entre une équipe de l'IRAMIS/NIMBE et deux équipes de l'I2BC@Saclay mettent en évidence l'affinité très forte de nanoparticules de silice pour des protéines de liaison de l'ARN présentant des séquences de base nucléique à motifs RGG (R = Adenine ou Guanine - Guanine-Guanine). Cette affinité est plus particulièrement renforcée lorsque celles-ci sont méthylées. Ces résultats sont importants pour le développement d'approches "safe by design", visant à minimiser l’écotoxicité des nanomatériaux, dès la conception d’un produit. |
|
Chez les organismes vivants, les processus de biominéralisation régulent la croissance des tissus minéralisés, tels que les dents, les os, les coquilles… Ces procédés restent fascinants à étudier pour une meilleure compréhension du monde naturel qui nous entoure et de sa diversité, d'autant plus que ces recherches peuvent contribuer à l'élaboration de procédés biomimétiques pour la réalisation de nouveaux matériaux. Une équipe interdisciplinaire française, à laquelle participe l'équipe du LIONS de l'UMR NIMBE, s'est intéressée à la bio-formation du carbonate de calcium, dont la structure complexe est encore largement incomprise. La texture complexe de matériaux naturels, observés auprès du synchrotron de l'ESRF par une méthode originale de diffraction de rayons X développée par l'Institut Frenel, est décrite et les résultats publiés dans la revue "Nature Materials". Un point de départ pour comprendre l'élaboration de ce composé, et définir les conditions physiques, chimiques et biologiques nécessaires pour produire de façon synthétique ce type de biominéraux. |