2011 Année de la Chimie à l'IRAMIS
|
Le dossier "Chimie à l'IRAMIS " au format PDF
|
 |
|
A coté de la recherche Nucléaire (fission et fusion), le CEA2 s’investi de plus en plus dans le développement des énergies "de demain" non émettrices de gaz à effet de serre et/ou renouvelables (pile à hydrogène, solaire, biomasse…) et prend en compte les problèmes environnementaux et sociétaux actuels (réchauffement climatique, valorisation du CO2…). Cette diversité d’activités repose sur une nécessaire interdisciplinarité scientifique dont la composante "chimie" n’est pas la moindre. Les quelques thématiques présentées ci-après illustrent l’investissement d’IRAMIS dans le domaine de la chimie liée aux énergies. |
- Nanosciences pour voitures roulant à l’hydrogène ?
- Cellules Photovoltaïques Organiques
- Des nanotubes de carbone pour le photovoltaïque
- Chimie de coordination des éléments f (uranium, thorium et lanthanides)
- Chimie sous rayonnement - Radiolyse
- Nouveaux matériaux pour les diodes électroluminescentes
- Le recyclage du CO2

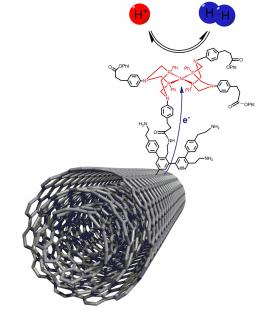
A l’heure où nous nous interrogeons sur les réserves fossiles de notre planète et que les dégâts environnementaux liés à leur combustion massive apparaissent aujourd’hui clairement, le remplacement du pétrole dans les transports par d’autres sources d’énergies moins polluantes est un défi majeur et difficile qui suscite aujourd'hui de nombreux travaux de recherche. Parmi les différentes voies explorées dans le cadre du transport automobile, une possibilité serait d’utiliser des moteurs électriques alimentés par des piles à hydrogène en remplacement des moteurs thermiques actuels. L'hydrogène serait produit par électrolyse de l'eau et donc à partir de l’électricité. Le transport "à l’hydrogène" est aujourd’hui techniquement réalisable mais son développement demande une réduction des coûts et l'amélioration de la fiabilité de certains constituants technologiques, en particulier les catalyseurs et les membranes.
Les électrolyseurs (production H2 à partir de l'eau) et les piles à hydrogène (production d'électricité) actuelles contiennent du platine, métal noble rare et cher, comme catalyseur pour l’oxydation ou la production de l’hydrogène. La substitution de ce platine par des métaux plus courants, abondants et bon marché est une nécessité économique, mais constitue un défi technologique majeur. Pourtant, dans le domaine du vivant, de nombreuses bactéries possédent des enzymes hydrogénases capables de réaliser ces réactions catalytiques avec une grande efficacité.
Avec leurs collaborateurs de Grenoble (IBS, IRTSV et LITEN), les chercheurs de l’IRAMIS développent des matériaux d’électrode à base de nanotubes de carbone et de catalyseurs biologiques (hydrogénases) ou de catalyseurs organométalliques inspirés de la structure de ces hydrogénases. Ces électrodes qui présentent une forte surface spécifique, une conductivité métallique et un catalyseur à base de nickel démontrent une activité catalytique prometteuse à la fois pour la production et l'utilisation de l'hydrogène et sont compatibles avec les technologies PEMFC (Proton Exchange Membrane fuel Cell) actuellement développées industriellement.
Parmi les différents types de piles, les plus intéressantes pour les applications dans le domaine du transport sont celles contenant une membrane polymère capable de jouer le rôle d’électrolyte solide. Dupont De Nemours commercialise une membrane à base de polymère perfluoré sulfoné, le Nafion®, largement utilisée malgré sa durée de fonctionnement limitée (5000 h) et sa fragilité mécanique. Des équipes d’IRAMIS essaient de répondre à ce problème en proposant un nouveau type de membrane fluorée : il s’agit d’un film polymère thermoplastique de type PVDF bombardé par les ions lourds rapides du GANIL (Grand Accélérateur National d'Ions Lourds à Caen) et radio-greffé par un polyélectrolyte le long des traces générées lors du passage des ions. Des nanocanaux de circulation sont ainsi créés privilégiant le transport des protons de l’anode vers la cathode. Ce type de membrane, testé en pile au LITEN, se révèle être un excellent matériau comparé au Nafion®.
Contacts : T. Berthelot (SPCSI), P. Chenevier (SPEC), M.-C. Clochard (LSI), B. Jousselme (SPCSI).
Fait marquant IRAMIS :
"Nanosciences et chimie bio-inspirée : un nouveau pas vers la production d’hydrogène sans platine"



Le rayonnement solaire constitue la ressource énergétique la mieux partagée sur la terre et la plus abondante. La quantité d’énergie libérée par le soleil pendant une heure pourrait suffire à couvrir les besoins énergétiques mondiaux pendant un an. Une partie de ce rayonnement peut être exploitée pour produire directement de l’électricité : c’est l’énergie solaire photovoltaïque. Le laboratoire de Nanostructures et Semi-Conducteurs Organiques (NaSCO) développe de nouveaux composants pour l’électronique moléculaire et plus particulièrement les Cellules Photovoltaïques Organiques (CPO).
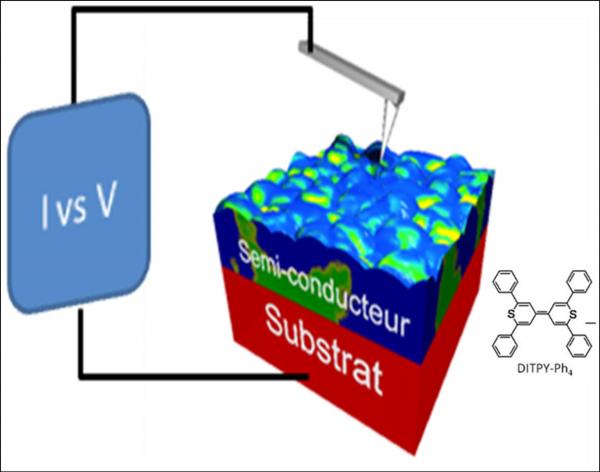
Ces matériaux, composés principalement de molécules organiques synthétisées en laboratoire, constituent une alternative efficace aux cellules solaires à base de silicium dont le cout énergétique et carbone à la fabrication est très important. Le groupe NaSCO, maitrise la fabrication des composants CPO, de la synthèse des molécules à la fabrication des composants et leurs caractérisations physico-chimiques. Les molécules synthétisées sont disposées entre deux électrodes sous forme de films minces (quelques nanomètres d’épaisseur, 1 nm = 10-6 millimètre) et leurs propriétés de transport de charges électriques sont étudiées au sein de dispositifs conventionnels notamment à l’aide d’un microscope à force atomique en mode détection de courant (CS-AFM). Dans ce contexte le laboratoire NaSCO a développé une famille de molécules DITPY (dithiopyrannilidene), qui a servi à l’élaboration de cellules photovoltaïques présentant une grande efficacité.
Contact : Laboratoire d'Innovation en Chimie des Surfaces et Nanosciences, IRAMIS/NIMBE/LICSEN
Ludovic Tortech ( Maître de conférences, Université Pierre et Marie Curie,
- Thèse Stéphane Berny (23/11/2010) : "Transferts de charges assistés par les dithiopyrannylidènes dans les cellules solaires et les hétérostructures magnétiques".
Stéphane Campidelli
CEA Saclay, IRAMIS/SPEC,
Laboratoire d'Electronique Moléculaire (LEM)
Les nanotubes de carbone constituent une classe relativement nouvelle de matériaux. Du fait de leurs propriétés physico-chimiques et électroniques hors du commun, ils sont considérés comme des éléments de choix pour la fabrication de polymères composites, pour la conversion d’énergie (photovoltaïque), pour l’électronique et les applications biologiques. En particulier, les nanotubes de carbone mono paroi présentent la propriété de pouvoir être soit métalliques soit semi-conducteurs selon la façon dont la feuille de graphène qui forme le tube est "enroulée" ; c’est une propriété très rare qui aiguise la curiosité de nombreux chercheurs.
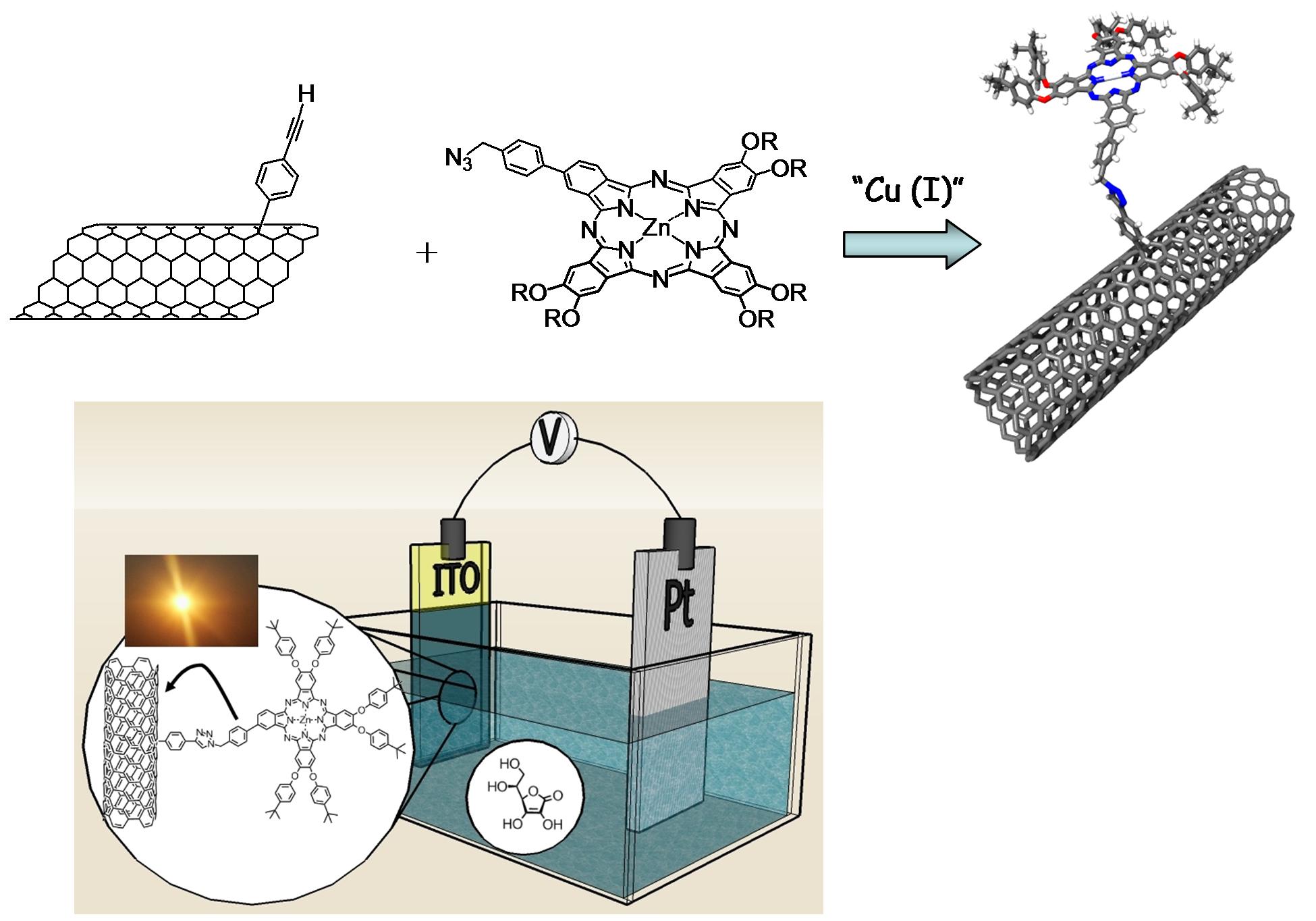
Les recherches conduites au Laboratoire d’Electronique Moléculaire portent essentiellement l’utilisation des nanotubes de carbone pour la nanoélectronique et la production d’énergie. Dans le but de transformer l’énergie lumineuse en énergie électrique (photovoltaïque), nous cherchons à fixer, sur les nanotubes, des molécules pouvant absorber la lumière et transférer des électrons à ces derniers. La figure présentée ci-dessous montre un exemple de fonctionnalisation des nanotubes de carbone avec des phtalocyanines ; ces composés ont été testés pour la fabrication d’électrodes photoactives.
Faits marquants associés :
Une fonctionnalisation chimique innovante pour des cellules solaires à base de nanotubes de carbone
Gaël Zucchi
CEA Saclay,
UMR SIS2M/LCCEf
Cette thématique pluridisciplinaire fait partie intégrante du domaine de l’électronique organique. Elle fait appel, entre autres, aux compétences relevant des domaines de la chimie et physico-chimie, de la physique des semi-conducteurs et de la caractérisation optique et électrique de dispositifs électroniques. Cet axe de recherche propose le design moléculaire, la synthèse, la caractérisation et l’utilisation de matériaux innovants comme composants actifs de diodes électroluminescentes organiques. Certains de ces matériaux contiennent des ions lanthanides qui possèdent des couleurs d’émission dans le visible et le proche infra-rouge d’une pureté incomparable. Les applications de ces dispositifs opto-électroniques sont très variées, elles vont de l’éclairage aux appareils à visée nocturne, en passant par le balisage et les écrans ultra-plats. En particulier, la très grande légèreté des dispositifs que ces matériaux permettent d’élaborer en fait des éléments de choix pour l’électronique embarquée.



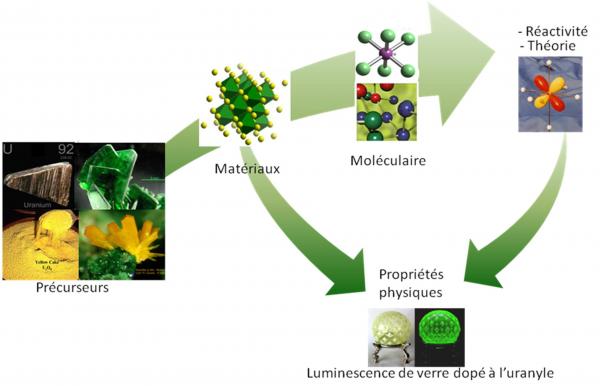
Les éléments f, lanthanides et actinides (principalement thorium et uranium), du fait de leurs orbitales 4f ou 5f et de la grande taille de leurs ions, s’associent à des molécules organiques (ligands) pour former des composés (ou "complexes") présentant des structures, des réactivités et des propriétés physiques remarquables, souvent différentes de celles des complexes des métaux de transition des séries d. Pour mettre en évidence la richesse réactionnelle de ces espèces qui se dégradent en présence de traces d’eau et d’oxygène, il faut les manipuler dans des milieux organiques anhydres et sous atmosphère inerte. Ces conditions permettent l’utilisation d’une large variété de ligands, souvent instables à l’air, qui favorisent le contrôle et la modulation des environnements stérique et électronique des ions métalliques et, de ce fait, la formation de complexes aux propriétés physico-chimiques désirées ou inattendues.
Le laboratoire de Chimie de Coordination des Eléments f (LCCEf) est spécialisé dans l’étude de la chimie des éléments f dans ces conditions particulières, et montre une prédilection pour l’uranium qui présente une faible radioactivité et de très nombreux attraits sur le plan chimique (nombreux ions, disponibilité des orbitales 5f, grande réactivité…).1 L’uranium est en outre un élément « modèle » permettant de mieux appréhender le comportement chimique des actinides les plus radioactifs, et d’apporter des informations utiles dans le domaine du nucléaire.2,3 Les recherches variées menées par le LCCEf sur les ions de ces métaux f,1 visent à exploiter leurs particularités chimiques sur les plans fondamentaux et appliqués dans les divers domaines de la chimie moléculaire (synthèse, structure, réactivité,1,4,5 activation de petites molécules6 (voir aussi : Le recyclage du CO2), de la catalyse, des matériaux, du magnétisme et de l’optoélectronique.7 (Voir aussi : Nouveaux matériaux pour les diodes électroluminescentes) Le couplage des études expérimentales et théoriques8 permet de relier les propriétés physico-chimiques des complexes à la nature de l’interaction métal-ligand en soulignant le rôle des orbitales f.
Références
1- a) Michel Ephritikhine, l’actualité chimique - août-septembre 2008 - n° 322 ;
b) Michel Ephritikhine et Martine Nierlich, la Chimie de Coordination des actinides, Clefs CEA n° 31, Hiver 1995-1996
2- Paul Rigny, l’actualité chimique - octobre 2010 - n° 345
3-Mise en évidence cristallographique de l’affinité et de la sélectivité des extractants polyazotés vis-à-vis des ions actinides et lanthanides, Brèves de l'IRAMIS n°119 (2002).
4- Diodes électroluminescentes organiques dopées avec des Lanthanides, Brèves de l'IRAMIS n°147 (2008).
5-a) Vers une renaissance de la chimie des sels d'uranyle, Journal Phase n°32 (Avril 2005).
b) Références Google "JC Berthet et Uranyle";
c) Un ion dans une cage ! Brèves de l'IRAMIS n° 184 (2009)
d) De nouveaux assemblages métal-organique à partir du citrate d'uranyle, Brèves de l'IRAMIS n° 163 (2009)
e) Une première : quatre uranyles d’un coup !, Brèves de l'IRAMIS n° 96 (2000)
6-a) Fixation de CO2 par une base azotée, Brèves de l'IRAMIS n°189 (2010)
b) Fait marquant IRAMIS Avril 2010 : Fabriquer du plastique sans pétrole et à partir du CO2 ?
c) Fantastique plastique, Défis du CEA n°152 (2010), p11-15.
7- Diodes électroluminescentes organiques dopées avec des Lanthanides, Brèves de l'IRAMIS n°172 (2008).
8- Fait marquant IRAMIS Janvier 2009 : Nouveau principe à 32 électrons : le cas de la famille de composés organométalliques (An = Th, Pa, U, Pu).
Contacts : Jean-Claude Berthet, Michel Ephritikhine et Pierre Thuéry.
CEA Saclay, IRAMIS- UMR SIS2M- LCCEf, Bât. 125, Gif-sur-Yvette 91191 Cedex.

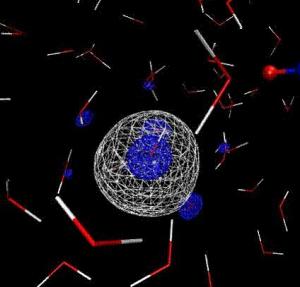
L’électron solvaté (représenté ici par l’intermédiaire de l’orbitale qu’il occupe dans l’eau) est une espèce clef de la radiolyse des liquides. Bien qu’il ait une durée de vie très courte (moins d’une microseconde) et qu’il soit constitué d’un unique électron entouré de molécules d’eau, c’est une espèce chimique à part entière.
La radiolyse, et plus généralement la "Chimie sous Rayonnement", est étudiée au sein de l’IRAMIS en interaction avec de nombreuses autres unités du CEA.
La rupture des liaisons chimiques causée par le fort dépôt d’énergie des rayonnements ionisants dans des matériaux tels que l’eau, les polymères, les liquides ioniques… provoque à long terme la formation de molécules (hydrogène moléculaire, eau oxygénée, acide chlorhydrique…) dont il faut connaître les rendements de production. La chimie qui se déroule quelques picosecondes après le passage du rayonnement est décisive pour le devenir des espèces chimiques. Le Laboratoire de Radiolyse s’intéresse tout particulièrement aux thématiques suivantes :
- Les conditions extrêmes de température et de pression qui sont souvent les conditions réelles de fonctionnement des réacteurs nucléaires,
- Les événements primaires en radiolyse des milieux concentrés ou soumis aux rayonnements de particules lourdes (alpha, protons, ions lourds),
- La radiolyse aux interfaces et dans les milieux poreux
- La biochimie radicalaire
- La radiolyse des polymères
- La radiolyse des molécules extractantes et des liquides ioniques
Les moyens utilisés pour l’irradiation vont des accélérateurs de particules ou source gamma. Pour l’analyse, les techniques spectroscopiques (de l’UV-Visible à l’InfraRouge), la chromatographie liquide et en phase gazeuse sont les techniques les plus couramment utilisées. De nombreuses collaborations nationales et internationales permettent par ailleurs d’étendre ce panel.
Lien internet sur la radiolyse au CEA : http://www-radiolyse.cea.fr/
Thibault Cantat,
CEA Saclay, IRAMIS/SIS2M, Laboratoire de Chimie de Coordination des Elements f (LCCEf)
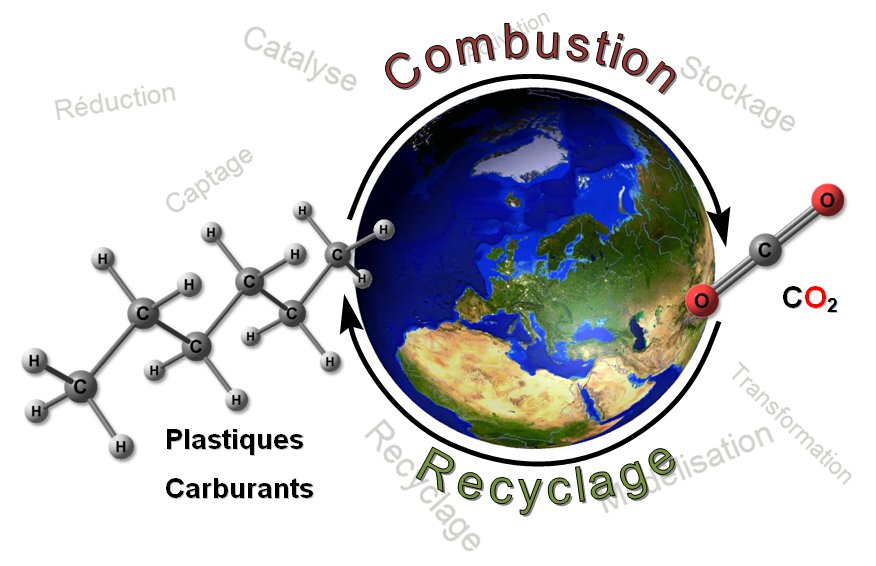
Le dioxyde du carbone (CO2) est le déchet organique ultime des activités humaines (industries, transport, bâtiment…). A l’heure de la raréfaction des combustibles fossiles, il est important de se détacher de la pétrochimie pour la préparation des plastiques, carburants… et de chercher à recycler le CO2 pour produire ces biens de consommation. Les chercheurs de l’IRAMIS concentrent leurs efforts sur le développement de nouvelles réactions de catalyse permettant de transformer le CO2 et sur la compréhension de l’interaction du CO2 avec la matière, à une échelle moléculaire.
Voir aussi le fait marquant : Fabriquer du plastique sans pétrole et à partir du CO2 ?